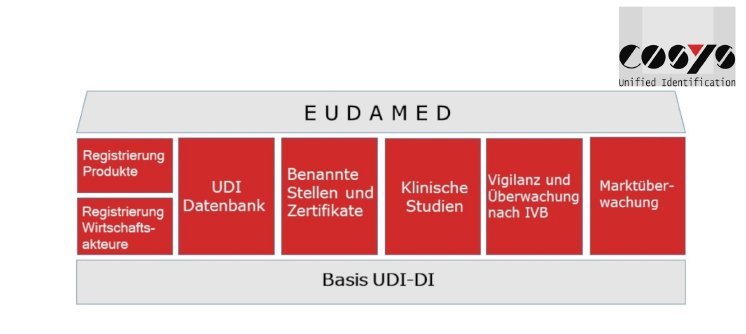
Ein wichtiger Bestandteil ist die europäische Datenbank (EUDAMED). Alle Wirtschaftsakteure müssen einen Zugang bei den Behörden beantragen. Die Akteure erhalten eine Single Registration Number (SRN). Mit dieser Nummer werden die Wirtschaftsakteure klar identifiziert und können auf die EUDAMED zugreifen.
Bevor ein Produkt in Umlauf gebracht wird, muss der Hersteller einen UDI-Code von der EUDAMED beantragen. Dafür registriert er das Produkt und erhält dann den Code. Welcher auf dem Produkt aufgebracht werden muss. Aber auch andere Wirtschaftsakteure müssen einen EUDAMED Zugang haben, weil die Produkte die gesamte Lieferkette über gescannt und gemeldet werden müssen. Die EUDAMED prüft den Code und gibt eine positive oder negative Rückmeldung zu dem Produkt aus.
Die EUDAMED Anforderungen sind in der MDR EU Verordnung beschrieben. Zugriff auf die Datenbank haben die europäische Kommission und die Mitgliedstaaten. Alle Wirtschaftsakteure haben eingeschränkten Zugang.
COSYS Software und EUDAMED
COSYS verfügt über Software, um die Eingaben an EUDAMED per Schnittstelle zu melden. Nach dem Einlesen der Daten werden diese in das COSYS Backend übertragen. Das Backend kann auf einem Server oder in der Cloud installiert werden. Anschließend übermittelt COSYS die Daten an die EUDAMED.
COSYS bietet neben der Software auch die Hardware, um die Codes zu erfassen. Zum Lesen der Codes eignen sich Smartphones, Tablets und MDE-Geräte.
Bis zum 26 Mai 2020 (MDR) bzw. 2022 (IVDR) müssen die ersten Wirtschaftsakteure (Produzenten, Importeuren, Großhändlern. Apotheken und Sanitätshäuser) eine Lösung geschaffen haben, um die Richtlinien umzusetzen.
Informieren Sie sich noch heute unter: https://www.cosys.de/pharma-eu-verordnung
Auch interessant:
EUDAMED
Medical Device Regulation
In-vitro-Diagnostika
UDI-Code