MünchBiopharmazeutika oder "biologicals" sind durch das Mitte der 70er Jahre entwickelte gentechnologische Verfahren der "recombinant DNA technology" hergestellte Arzneimittel. Im Gegensatz zu den klassischen niedermolekularen Arzneien wie z.B. Aspirin®, welche aufgrund ihrer einfachen Molekülstruktur im Rahmen simpler chemischer Synthesen hergestellt werden können, handelt es bei der Gruppe der Biopharmazeutika um hochkomplexe Polypeptide und Proteine. Der Herstellung von Biopharmazeutika wie etwa Avastin® oder Herceptin® von Roche/Genentech oder Neulasta® von Amgen liegt daher ein hochkomplexer und aufwendiger Herstellungsprozess zugrunde, der auf der natürlichen Biosynthese von Proteinen und Polypeptiden in Mikroorganismen (z.B. E. coli) oder in Zellkulturen (z.B. Ovarienzellen des Chinesischen Hamsters) beruht. Der Komplexität dieses Herstellungsprozesses, sowie den wesentlich höheren Entwicklungskosten ist es auch zuzuschreiben, dass die meisten Biopharmazeutika in die Sparte der sogenannten "Hochpreismedikamente" fallen. So belaufen sich die jährlichen Behandlungskosten mit Herceptin® zum Beispiel auf $US 60.000.
Es sind zum Teil diese enormen Behandlungskosten und die damit verbundenen Umsätze, welche die Entwicklung von biopharmazeutischen Nachahmerprodukten, sogenannten Biosimilars, interessant erscheinen lassen. Dies gilt trotz der im Vergleich zu klassischen Generika wesentlich höheren Entwicklungskosten für Biosimilars. Während die Entwicklung eines klassischen Generikums mit 0,5-5 Mio $US zu Buche schlägt, liegen die Aufwendungen für die Biosmiliar Entwicklung, bei in etwa Vergleichbaren Entwicklungszeiten, mit 20-80 Mio $US um ein vielfaches höher.
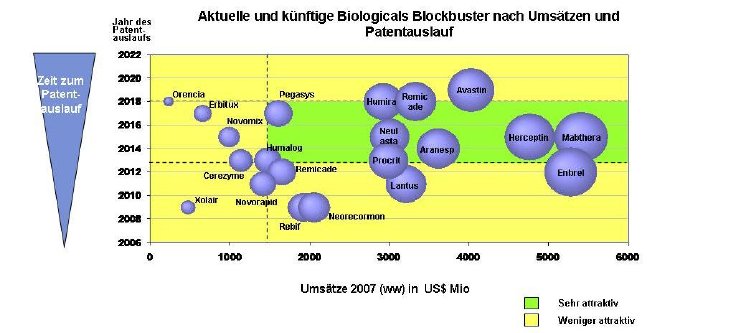
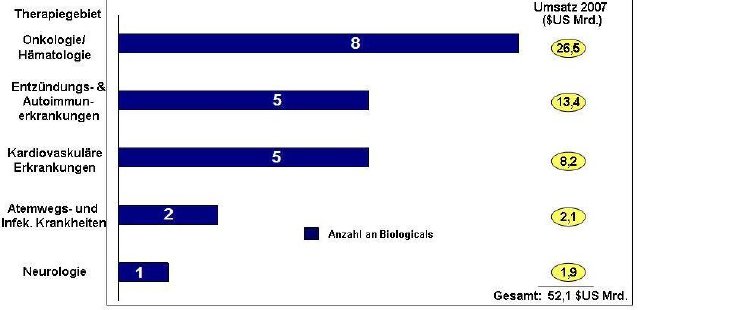
Mit Sandoz-Hexal's Omnitrope und Valtropin von Biopartners (beides Nachahmungen des Wachstumshormons Somatotropin) gelangten im Jahre 2006 die ersten beiden Biosimilars in Europa zur Zulassung. Derzeit befinden sich 11 Biosimilars auf dem deutschen Markt, darunter Nachahmerpräparate von Insulin, Interferon ? und ß sowie des "Granulocyte Colony Stimulating factor" (GCSF). Weltweit sind momentan über 150 biotechnologisch produzierte Substanzen auf dem Markt und ca. 370 weitere befinden sich in der Entwicklung. Innerhalb der nächsten 10 Jahre (2009-2019) verlieren insgesamt 21 dieser Biologicals im Wert von über 50 Mrd $US (basierend auf den Verkaufserlösen des Jahres 2007) ihren Patentschutz. Jährlich werden dabei durchschnittlich ca. 5,8 Mrd $US an Umsätzen frei, die zumindest teilweise den Entwicklern entsprechender Biosimilars zufließen könnten. Die Therapiegebiete, welche die meisten Patentausläufe verzeichnen, sind die Onkologie, Entzündungserkrankungen und Kardiovaskuläre Erkrankungen.
Die Chance, an diesen Umsätzen zu partizipieren bietet sich natürlich nicht nur den aktuellen Biosimilarentwicklern, wie etwa Sandoz-Hexal, TEVA oder Biopartners, sondern natürlich auch den Unternehmen, die aufgrund Ihres Know-hows die Entwicklung von Biosimilars als neues Geschäftsfeld entwickeln könnten. Zu beachten sind allerdings die derzeit noch unklaren regulatorischen Gegebenheiten für den US Markt. Während die EMEA für die Entwicklung und Zulassung von Biosimilars in Europa bereits 2005/2006 klare Richtlinien erstellt hat, stehen diese in den USA noch aus. Gegenwärtig wird diesbezüglich eine Entscheidung der FDA für das Jahr 2009 erwartet. Das einzige bist heute in den USA zugelassene Biosimilar Präparat Omnitrope®, ein Wachstumshormon, erhielt seine Zulassung im Rahmen eines Ausnahmeverfahrens.